40年に渡り、マリファナはアヘンやコカインより規制が厳しく、スケジュールIの薬物として分類されてきました。ですので、今週、アメリカ食品医薬品局(FDA)が大麻草由来の医薬品を承認したのは画期的出来事です。
承認されたのはてんかん治療のために開発したCBD
Epidiolex、イギリスが拠点の医薬品会社、GW Pharamaceuticalsがてんかん治療のために開発したCBDの精製型です。FDAが他の成分、ドロナビノールなどの合成カンナビノイド(合成THC)を承認する中、政府がカンナビスサティバ(大麻草)の医療的効果を承認したことはありませんでした。
言うまでもなく、医療用大麻にとって大きな一歩です。CBD、てんかんを持つ子供のために、親が罰則のリスクを冒して入手していた薬が、もうすぐ一般的に入手可能になるでしょう。
「私たちはEpidiolexは他のてんかん医療薬と同じ、ScheduleⅥかScheduleⅤに分類されるようになると信じています。」
「ここ数日間はとても忙しかったです。」GW Pharmaceuticalsとアメリカの子会社であるGreenwich BiosciencesのIR担当副社長Stephen Schultzは述べました。「エキサイティングで歴史的な出来事でした。」FDAの発表は、想定通りの反響から、Epidiolexの価格についてまで様々な憶測を生みました。GW Pharmaのほかの製品についても話題にあがりました。
LeafyはSchultz氏とFDAの重要な決断、Epidiolexが患者に使用可能になった今、次はどうするのか、という話をしました。下記に内容をまとめました。
Leafy:今週のFDAが大麻草由来で子供のてんかんにも効果のあるEpidiolexを承認したことは大きなニュースになりました。まずEpidiolexの主な効果を教えていただけますか?
Schult:GW Pharamaceuticalsと子会社のGreenwich Biosciencesは、精製されたCBDであるEpidiolexの完全臨床開発プログラムを実施しました。このプログラムでは、3つのプラセボコントロールに関する臨床試験で成り立っています。そのうちの3つは、New England Journal of MedicineとThe Lancetのトップ記事に掲載されています。
データは広範囲に渡り、ドラべ症候群とレノックス・ガストー症候群、どちらもてんかんを引き起こす症状に効果がありました。これらの試験から安全性と有効性、双方に関する詳細な情報が得られました。
我々は主要評価項目で、発作条件の異なるタイプでも発作減少率が統計的に低下していることがわかりました。他の薬と合わさることによる副作用はあります。詳細はFDAによる製品のラベルと、New England Journal of MedicineおよびThe Lancetの記事で詳しく説明されています。
これらの患者は一般的に複数の医薬品を服用しています。我々の臨床試験で患者達は平均で10種類の薬を試し、失敗しています。製品を試してもらう前は平均で3種類の薬を常用していました。
FDAがEpidiolexを認証した今、次は何が起こるでしょう?
患者にドラッグの入手が可能になった時はどうなるのでしょう?
最初のステップは承認であり、我々はそれよりずっと遠い所にいます。次のステップは、DEAが昨日の認証から90日以内に製品の薬物分類を変更することです。薬物分類の変更はFDAによる分析のあとにDEAに委ねられるでしょう。DEAは新薬情報に含まれる情報と分析に基づき分類します。この過程も90日ほどかかると予想しています。
この薬、Epidiolexは絶対に分類しなおされるべきで、ScheduleIから外されるべきです。乱用分析研究の意見は4月19日の公開FDA諮問委員会会議に反映されました。分析家はこのCBDの乱用性はとても低く、我々はScheduleIからははずされるだろうと予想しています。
CBDをSchedule IIに移行するだけでなく、より大きな変化を期待していますか?
再分類はScheduleIからScheduleⅤの間で行われ、EpidiolexはScheduleⅤかScheduleⅥ、他の抗潰瘍薬、ベンソジアゼピンと同じように分類されると思っています。
我々は、FDAの試験がてんかんと関係していたと認識していますが、明らかにCBDにはそれ以上の医療効果があります。Epidiolexの承認は、慢性的な痛み、不安、およびその他の症状にも使用できるようになるのでしょうか?
良い質問です。しかし、FDAは特定の患者だけへの結果を要求しています。それぞれ違った症状を持つ患者と、違った治療方法では同じ薬でも効果は違ってくるでしょう。Epidiolexのように承認された薬は科学的根拠によって区別されているため、我々が開発した臨床データに基づき区別する必要があります。
医薬品の処方は患者とその医師の間で行われていますが、Greenwich Biosciencesはドラべ症候群とレノックス・ガストー症候群の患者以外には薬を宣伝しません。特定患者以外への宣伝は不適切であり、繰り返しますが、医師とその患者の間のみで薬を処方するという決定があります。
このFDAの承認に関して最も注目すべき事柄の一つは、規制当局が実験室で成分を合成する代わりに、大麻草から実際に得た成分の薬を初めて処方したことです。それはGW Pharmaが思うほど重要なことなのでしょうか?重要だとしたらなぜなのでしょうか?
我々にとって、それが重要なのは、我々が行ってきた植物由来のカンナビノイドを使用し、薬を作り出す方法に意味があったということです。FDAが正しく順調に承認すれば、新たな道が開けるのです。
それは我々、この分野で働くことを計画している人々にも、Epidiolexを含め、CBD製品が他の医薬品と同様に進歩し、研究ができるという自信になるのです。
人々が思うように、Epidiolexの承認は、マリファナコミュニティ、特に潜在的に有益な他のカンナビノイドを含む「大麻草全体」からの抽出物の重要性を強調している人々の間に不安を生みました。大麻草全体の利益に執着している人々はそれらの製品の抑制を心配しています。そのことについてはどう思いますか?
まったく関係ありません。我々は、他のCBD製品について言及することはないと考えています。
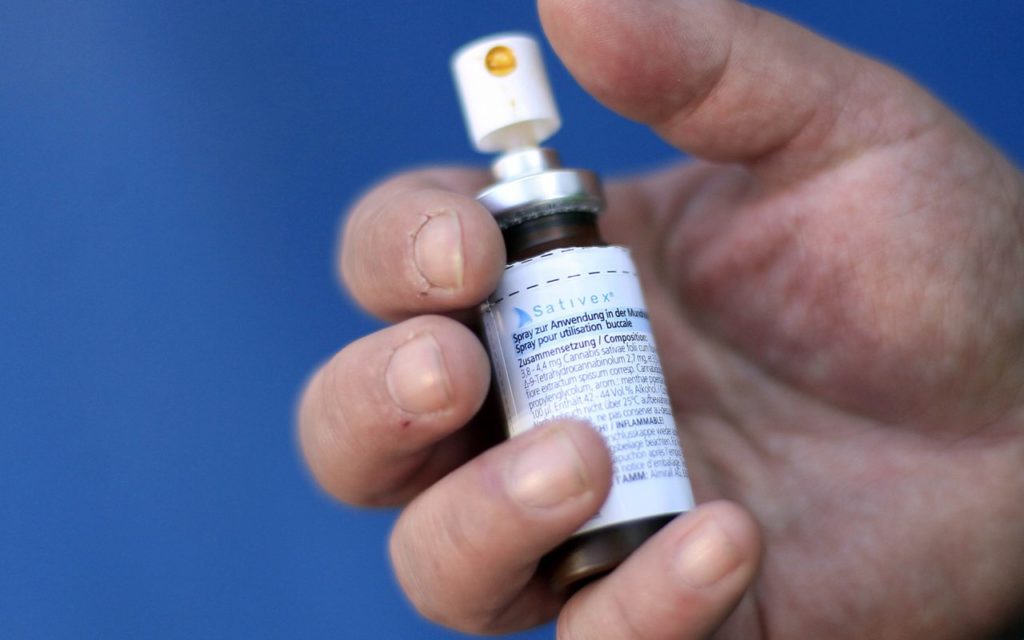
「我々はSativexをアメリカに持ち込み、臨床試験を行い、できるだけ早くFDAに申請したいと考えています。」
我々は医師や患者が、難病治療のためにCBD薬を心待ちにしていると信じ、薬の開発を行ってきました。摂取するたびにすぐ変化が起こるものではありません。これは他の治療薬にも言える問題です。さきほど話した科学的証拠、New England Journal of Medicineの記事、The Lancetの記事のような情報提供が、医師がより詳細に薬や使用方法を理解する手助けになります。また、患者の保険適用に応じて、払い戻しができる可能性もあります。
我々は、そのような特性を持つこの製品の重要性と需要を考え、このようなアプローチ方法をとっています。
私が見たもう一つの懸念は、治療費と関係があります。Epidiolexが保険でカバーされているかもしれないと述べましたが、すでにNew York TimesはEpidiolexが月に2,500ドルから5,000ドルの間で保険適用ができると記載しています。それが正確な情報なら、その適用を受ける人々は何をすればもっと手頃に入手が可能になるのでしょうか?
我々は薬の価格をまだ決めておらず、DEAの調整が終わるまでは決定しないでしょう。ですので、価格の推測についてコメントするのは難しいですが、New York Timesの予想は現時点で考えているよりも、おそらく高いと思います。
私たちの薬が使用可能になれば、CBD製品を希望し、必要とするできるだけ多くの患者と医者が利用できるようにしたいと考えています。それを可能にするためのさまざまな戦略がありますが、まだ開発中のものがたくさんあるので、詳細はお教えできません。我々の会社の目的は、ドレベ症候群とレノックス・ガストー症候群の患者が必要に応じて薬が入手できるようになることです。
ある州が大麻を合法化しても、価格が下がるまで、消費者はより安価な製品を手に入れるため、不法な入手方法をとることがあります。GW Pharmaceuticals は、すでにある州では成人や医療用として薬局で手に入る高濃度のCBDオイルとの競争は考えているのでしょうか?
患者や医師との話し合いでは、FDAが承認した医薬品に対する大きな需要があります。これは我々が薬を開発した理由の1つであり、ドラべ症候群およびレノックス・ガストー症候群の発作の治療のため、医師か患者によって選択される製品であると確信しています。
そう言った意味で、薬の使用の決定は患者と医師の間で行われます。彼らが特定の状況により選んだ最善の入手ルートは、我々ではなく彼らのためです。
GW Pharma が開発中のほかの大麻由来の薬はあるのか?
我々は、てんかん発作に抵抗するEpidiolexの研究を継続するつもりです。実際には現在、一次合併症の弊害として起こる発作、結核性硬化症複合体(TSC)と呼ばれる症状への試験を行っています。2019年にはこのデータがまとめられることを期待しています。他には、てんかんへの抵抗治療の追加臨床試験を開始することによって、Epidiolexのラベルの情報を書き加えていく考えです。
Sativexとは?
Epidiolexを超え、アメリカの地平線の向こうで非常に素晴らしい製品があります。多発性硬化症による痙性の治療のためヨーロッパの多くの国で使用が認可されているSativexです。今はとてももどかしい状況です。我々はそれをアメリカに持ち込み、臨床開発に投入し、できるだけ早くFDAに申請したいと考えています
Sativex以外にも、早期にすでに検証を経たいくつかの製品の臨床評価を拡大することに関心を抱いています。これらの製品には、統合失調症の治療効果が含まれています。脳腫瘍の非常に稀な形態である神経芽細胞腫、自閉症スペクトラム障害は特に若い女児に影響を与えます。非常に改善が困難な自閉症スペクトラム障害である、レット症候群については、今年後半に臨床研究を開始する予定です。
基本的に、これが我々の科学を発展させる方法です。カンナビノイドを個別、または組み合わせて、 SativexがCBDとTHCの組み合わせかどうかを実証し、それらを最終的に臨床試験で異なる治療に効果があるのか評価します。その後、規制当局に持ち込み、使用を認めてもらうことを目標としています。
出典:Leafly

Be the first to write a comment.